规绳矩墨——医疗合规那些事儿之四:药械使用管理及物流合规
2022.07.03 余苏
“药以安为先,安以质为本,质以诚为根。”医疗合规中一个不可忽视的环节就是药械使用管理及物流合规。在2018年长春长生的假疫苗事件中,国家药监局重拳出击,开出91亿罚单,涉案的高俊芳等14名责任人被终身市场禁入并被依法追究刑事责任。这再次为我们敲响警钟,安全、有效的药品和医疗器械是保障人民群众生命安全和身体健康的重要支撑。
随着《医疗器械监督管理条例》《医疗器械使用质量监督管理办法》《医疗器械经营监督管理办法》等法律法规的出台,我国已经构建起了全面的药械使用管理及物流合规的法律体系。
本文将结合相关法律规定和行政处罚案例,介绍药械使用管理及物流中涉及的产品质量管理、仓储管理、物流环节的合规要点以及不良事件应对要点,并提供相关合规建议以供参考。
一、产品质量管理合规
“医疗合规千万条,质量管理第一条。”药品和医疗器械的质量是守护人民群众健康的第一道防线。医疗卫生机构应当建立健全与所经营医疗器械相适应的质量管理体系并保证其有效运行。在实践操作中,可以重点关注以下几类医疗器械的质量管理要求:
医疗器械种类 | 合规要点 |
一次性使用的医疗器械 | 《医疗器械监督管理条例》第四十九条第二款:一次性使用的医疗器械不得重复使用,对使用过的应当按照国家有关规定销毁并记录。 |
需要定期检查的医疗器械 | 《医疗器械监督管理条例》第五十条:医疗器械使用单位对需要定期检查、检验、校准、保养、维护的医疗器械,应当按照产品说明书的要求进行检查、检验、校准、保养、维护并予以记录,及时进行分析、评估,确保医疗器械处于良好状态,保障使用质量。 |
购买、受让、受赠的医疗器械 | 《医疗器械使用质量监督管理办法》第八条:医疗器械使用单位应当从具有资质的医疗器械生产经营企业购进医疗器械,索取、查验供货者资质、医疗器械注册证或者备案凭证等证明文件。对购进的医疗器械应当验明产品合格证明文件,并按规定进行验收。对有特殊储运要求的医疗器械还应当核实储运条件是否符合产品说明书和标签标示的要求。 《医疗器械使用质量监督管理办法》第二十条:受让方应当参照本办法第八条关于进货查验的规定进行查验,符合要求后方可使用。 《医疗器械使用质量监督管理办法》第二十一条:受赠方应当参照本办法第八条关于进货查验的规定进行查验,符合要求后方可使用。 |
第二类、第三类医疗器械 | 《医疗器械监督管理条例》第四十五条:从事第二类、第三类医疗器械批发业务以及第三类医疗器械零售业务的经营企业,还应当建立销售记录制度。 |
【行政处罚案例】
在产品质量管理环节,医疗卫生机构常出现的不合规事项有:(1)在采购环节中,采购渠道不规范,索证索票工作不严谨,未按要求建立或执行进货查验制度;(2)在使用环节中,使用未经注册的产品,重复使用一次性器械产品,使用过期、失效产品。
例如,在哈市监械罚〔2022〕002号1一案中,当事人哈尔滨某医疗器械公司从不具备合法资质的网上个人处购进不符合强制性标准的“医用外科口罩”。最终被哈尔滨市市场监督管理局没收不符合强制性标准医疗器械“医用外科口罩”30000支并被罚款114000元、没收违法所得7500元。
【合规建议】
我们建议医疗卫生机构在药械的产品质量管理环节中除了要重视查验之外,还需要特别重视记录,尤其是留下书面记录资料,具体而言可以采取以下措施:
(1)在入库验收环节,医疗卫生机构应建立购买、受让、受赠医疗器械的进货查验制度。
(2)在期限管理环节,医疗卫生机构应按照规定存放医疗器械,建立有效期、使用期限管理制度,避免使用失效、过期、淘汰的医疗器械。
(3)在质量检查环节,医疗卫生机构应对须定期检查的医疗器械进行检查、维护医疗器械并予以记录,同时对使用期限长的大型医疗器械单独建档管理。
(4)在凭证记录环节,要确保凭证记录的真实性、准确性、完整性、可追溯性,从事第二类、第三类医疗器械批发业务以及第三类医疗器械零售业务的经营企业,还应当建立销售记录制度。
二、仓储管理合规
仓储管理是药械使用管理中的重要环节,实践中医院、医药公司、医疗器械公司等主体在存储药品和医疗器械时可能因管理不严格、操作不规范而导致药品和医疗器械在不适宜的温度、湿度下贮存,进而导致相关药械失活、失效甚至被污染。
【行政处罚案例】
在仓储管理环节,医疗供应链相关企业和机构出现的不合规事项主要是未按照产品说明书和标签标示要求贮存医疗器械。
例如,在穗海市监处字﹝2022﹞38号2一案中,当事人广州某健康药房经营场所的温湿度表显示温度为27℃,但货架上摆放的扫描式葡萄糖监测系统传感器套装要求存放的温度为4℃至25℃。当事人因未按照医疗器械说明书和标签标示要求贮存医疗器械,被罚款5000元。
【合规建议】
我们建议医疗卫生机构在药械的仓储管理中可以关注以下要点:
(1)在仓储管理环节,医疗卫生机构应当建设整洁、干燥、避光、通风的仓储区域,对待验区、合格品区、不合格品区、发货区等区域实行分区管理,例如可采用色标管理,设置待验区为黄色、合格品区和发货区为绿色、不合格品区为红色;重点关注药械的存储温度和湿度须符合产品说明书和标签标识的要求,同时采取“先产先出、近期先出、易变先出”的仓储管理办法。
(2)在冷链贮存环节,医疗卫生机构应当根据生产经营的品种和规模,建立科学的冷链贮存体系。
(3)在仓库安全环节,医疗卫生机构应重点关注仓库的防火安全。
(4)特殊医疗器械的存储管理:
针对大型医用设备,《医疗器械监督管理条例》规定,医疗器械使用单位配置大型医用设备,应当符合国务院卫生主管部门制定的大型医用设备配置规划,与其功能定位、临床服务需求相适应,具有相应的技术条件、配套设施和具备相应资质、能力的专业技术人员,并经省级以上人民政府卫生主管部门批准,取得大型医用设备配置许可证。
针对麻醉药品及第一类精神药品,《麻醉药品和精神药品管理条例》规定,麻醉药品和第一类精神药品的使用单位应当设立专库或者专柜储存麻醉药品和第一类精神药品。专库应当设有防盗设施并安装报警装置;专柜应当使用保险柜。专库和专柜应当实行双人双锁管理。
三、物流合规
2022年6月10日,国家药监局综合司发布《医疗器械经营质量管理规范附录:第三方物流质量管理(征求意见稿)》(以下简称“《征求意见稿》”)。医疗器械第三方物流合规提上日程,《征求意见稿》共八章三十九条,分别从质量管理体系、人员与培训、设施与设备、计算机信息系统、委托方式与质量责任、特殊类别管理要求六个方面对医疗器械第三方物流提出了新的合规要求。
【行政处罚案例】
在(岷)市监处罚〔2022〕3号3一案中,当事人甘肃某医疗器械公司在向医院供货时,其用于储存第二类医疗器械的冷库、冷藏柜未按要求进行验证,不具备第二类医疗器械冷链储存、运输条件且当事人无法提供与该批次医疗器械冷链运输记录相应的冷链确认单,故被岷县市场监督管理局罚款30000元。
【合规建议】
我们认为在物流合规环节可以关注以下要点:
(1)资质要求:物流服务商须取得《道路运输经营许可证》。同时我们注意到《征求意见稿》还要求物流服务商须取得《医疗器械经营许可证》或经营备案凭证。
(2)业务要求:配备与医疗器械运输服务相适应的设备设施、人员,有全程可追溯的信息管理平台对运输设备、运输产品、承运人员、运输进度等信息进行追踪管理。
(3)特殊医疗器械的运输:有特殊运输要求的医疗器械须保证在运输途中符合温度、湿度等要求。
四、不良事件应对
医疗器械不良事件,是指已上市的医疗器械,在正常使用情况下发生的,导致或者可能导致人体伤害的各种有害事件。2022年3月,国家药品不良反应监测中心发布的《国家医疗器械不良事件监测年度报告(2021年)》显示,2021年国家医疗器械不良事件监测信息系统接收到医疗器械不良事件报告65万余份,比上年增加21.39%;28个省(自治区、直辖市)的医疗器械不良事件报告县级覆盖率达到100%。
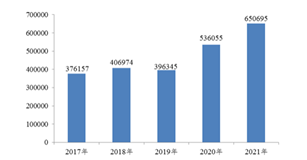
图1 2017-2021年全国医疗器械不良事件报告数量
这提示我们医疗器械不良事件的监测与评价工作绝不是一件小事,医疗供应链的相关企业和机构切不可抱有侥幸心理。建立一套科学合理、行之有效的医疗器械不良事件监测与评价体系,可以减少或者避免同类医疗器械不良事件的重复发生,促进医务人员科学、合理用械,规范医疗操作行为,降低患者、医务人员和其他人员使用医疗器械而造成伤害的风险,有效保障广大人民群众用械安全,促进我国医疗器械产业的持续、健康发展。
【行政处罚案例】
在清市监处〔2020〕177号4一案中,当事人清河县某药店连锁公司分店未按要求建立医疗器械不良事件监测工作制度,经复查,当事人仍未按要求建立医疗器械不良事件监测工作制度,故被清河县市场监督管理局罚款5500元。
在沪监管闵处字(2019)第122019015690号5一案中,当事人上海某医疗器械公司主要从事第三类医疗器械批发,理应加强对所经营的医疗器械的质量管理及对所经营的医疗器械开展不良事件监测,但当事人自取得医疗器械经营许可证之日至案发时,一直未开展医疗器械不良事件监测,同时也未严格遵守医疗器械不良事件监测制度。故而被上海市闵行区市场监督管理局罚款5000元。
【合规建议】
根据《医疗器械监督管理条例》《医疗器械不良事件监测和再评价管理办法》和《医疗器械召回管理办法》的规定,我们认为在不良事件应对过程中可以采取以下措施以防范和化解潜在风险:
(1)不良事件监测制度:建立药械不良事件监测体系,配备相关机构和人员。
(2)在三类情形下应主动开展已上市医疗器械再评价工作:①根据科学研究的发展,对医疗器械的安全、有效有认识上的改变;②医疗器械不良事件监测、评估结果表明医疗器械可能存在缺陷;③国务院药品监督管理部门规定的其他情形。
(3)不合格或缺陷产品的处理:在发现不合格或缺陷产品后立即停止生产,通知相关企业、使用单位和消费者停止经营和使用,召回已销售的器械,同时要记得向监管部门报告。
习近平总书记2021年3月在福建考察时强调:“现代化最重要的指标还是人民健康,这是人民幸福生活的基础。”医疗供应链的相关企业和机构只有将药械使用管理和物流合规摆在重要位置,慎始敬终,医疗健康事业才能行稳致远,“健康中国”的顶层设计才能逐渐走入寻常百姓家。
1. https://law.wkinfo.com.cn/administrative-punishment/detail/MkUwNTM0MjY4MTM%3D?searchId=8d1c9c2db1f84ce8ac1c01a0b230ced9&index=1&q=%E5%93%88%E5%B8%82%E7%9B%91%E6%A2%B0%E7%BD%9A%E3%80%942022%E3%80%95002%E5%8F%B7&module=
2. https://law.wkinfo.com.cn/administrative-punishment/detail/MkUwNTEzNDA1NzI%3D?searchId=2a4fe43f243944fcaaf233b89e1be8c0&index=1&q=%E7%A9%97%E6%B5%B7%E5%B8%82%E7%9B%91%E5%A4%84%E5%AD%97%EF%B9%9D2022%EF%B9%9E38%E5%8F%B7&module=
3. https://law.wkinfo.com.cn/administrative-punishment/detail/MkUwNTA4MTEwNzc%3D?searchId=60a1cb72ccfb40c3b03248ba2f5f35a9&index=1&q=%EF%BC%88%E5%B2%B7%EF%BC%89%E5%B8%82%E7%9B%91%E5%A4%84%E7%BD%9A%E3%80%942022%E3%80%953%E5%8F%B7&module=
4. https://law.wkinfo.com.cn/administrative-punishment/detail/MkUwMzgwNjUwNjI%3D?searchId=7973c7296b1a4e9f9e82441d5312050e&index=1&q=%E8%8D%AF%E5%BA%97%E8%BF%9E%E9%94%81%E5%85%AC%E5%8F%B8%E5%88%86%E5%BA%97%E6%9C%AA%E6%8C%89%E8%A6%81%E6%B1%82%E5%BB%BA%E7%AB%8B%E5%8C%BB%E7%96%97%E5%99%A8%E6%A2%B0%E4%B8%8D%E8%89%AF%E4%BA%8B%E4%BB%B6%E7%9B%91%E6%B5%8B%E5%B7%A5%E4%BD%9C%E5%88%B6%E5%BA%A6%205500&module=
5. https://law.wkinfo.com.cn/administrative-punishment/detail/MkUwMDY4NjE5MzA%3D?searchId=ac87338544cf4f99a3319c84541154e7&index=1&q=%E6%B2%AA%E7%9B%91%E7%AE%A1%E9%97%B5%E5%A4%84%E5%AD%97%EF%BC%882019%EF%BC%89%E7%AC%AC122019015690%E5%8F%B7&module=












